Для кого эта статья:
- студенты и школьники, изучающие химию
- преподаватели и методисты, работающие в области химического образования
- профессионалы и специалисты в области органической химии и химической промышленности
Для начала вспомним, что это за класс веществ такой — алкены.
Алкены — это непредельные углеводороды, в молекуле которых между атомами углерода имеется одна двойная связь.
Алкены обладают высокой реакционной способностью, поэтому в природе встречаются значительно реже, чем предельные углеводороды (алканы). Для получения алкенов используют в качестве исходного вещества предельные углеводороды и некоторые их производные.
По структуре алкены похожи на алканы. Повторить теорию по этой теме поможет наша статья «Общая формула алканов».
Промышленные способы получения алкенов
Получение алкенов - способы синтеза ненасыщенных углеводородов: дегидратация спиртов кислотами (например, H₂SO₄), дегидрогалогенирование галогеналканов спиртовым раствором щёлочи (например, KOH), дегалогенирование дигалогеноалканов цинком или магнием.
Примеры:
- Дегидратация: CH₃CH₂OH → CH₂=CH₂ + H₂O (с конц. H₂SO₄)
- Дегидрогалогенирование: CH₃CH₂Br + KOH → CH₂=CH₂ + KBr + H₂O (в спирте)
- Дегалогенирование: CH₂Cl-CH₂Cl + Zn → CH₂=CH₂ + ZnCl₂
Термический крекинг алканов
Термический крекинг — это процесс переработки нефти и ее фракций путем термического разложения углеводородов с получением веществ с меньшей молекулярной массой.
При термическом крекинге алканов образуется смесь алканов и алкенов. Например, при разложении октана — бутан и бутен.
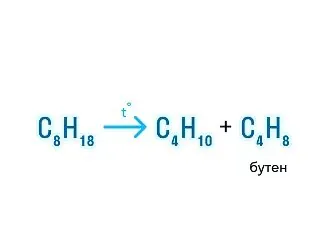
При термическом разложении алканов исходная молекула может делиться на два продукта с разным количеством атомов углерода в цепи.
Например:
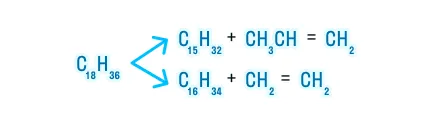
Дегидрирование алканов
Реакция дегидрирования — это реакция, в результате которой от молекулы органического соединения отщепляется молекула водорода.
Реакция протекает при нагревании и в присутствии катализатора (Cr2O3, Pt и других), а продуктом является вещество с таким же количеством атомов углерода в цепи.
Пример получения алкена из алкана:
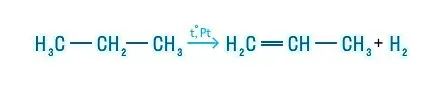

Лабораторные способы получения алкенов
Дегидратация спиртов
Реакция дегидратации — это реакция отщепления молекулы воды от органического соединения.
Такой вид реакции получения алкенов протекает в присутствии водоотнимающего средства — концентрированной серной кислоты H2SO4 (конц.) — и при нагревании выше 140°.
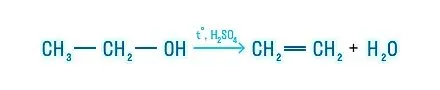
Если исходная молекула спирта является несимметричной, то отщепление молекулы воды протекает по правилу Зайцева.
Иными словами, водород необходимо отщеплять от того углерода, где его уже меньше.
Рассмотрим получение алкенов из спиртов подробнее на примере гидратации бутанола:
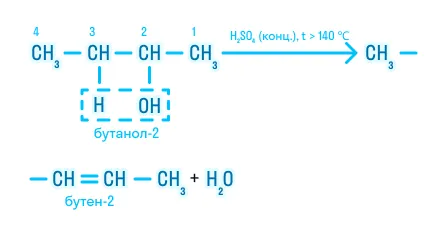
Атом углерода под цифрой 1 содержит три атома водорода, а атом углерода под цифрой 3 — один. Значит, по правилу Зайцева атом водорода в реакции дегидратации отщепляется от атома углерода под цифрой 3. Соответственно, двойная связь образуется между вторым и третьим атомами углерода.
Алкены активно используются в производстве полимеров, таких как полиэтилен и полипропилен. Подробнее о типах пластмасс и их применении можно узнать в статье «Пластмасса».
Дегидрогалогенирование моногалогенпроизводных
Отщепление галогеноводорода происходит при нагревании галогеналканов в присутствии концентрированного спиртового раствора щелочи:
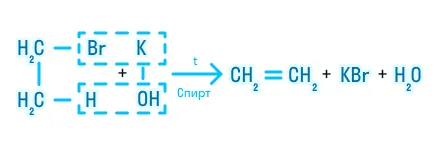
Иногда спиртовой раствор щелочи не записывают в реагирующих веществах:
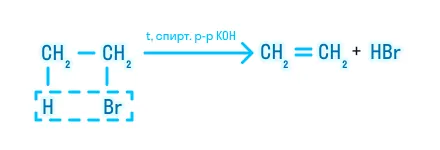
Отщепление галогеноводорода в несимметричных молекулах протекает также по правилу Зайцева:
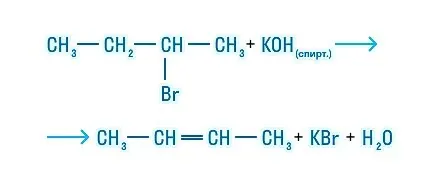
При дегидрогалогенировании 2-бромбутана мы видим, что у третьего атома углерода только один водород, а у первого — три. Водород отщепляется от третьего атома углерода.
Дегалогенирование дигалогеналканов
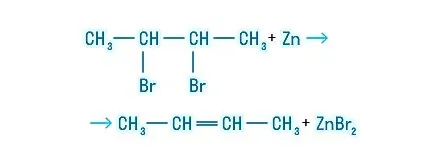
При наличии двух атомов галогена у соседних атомов углерода в молекуле алкана происходит их отщепление при взаимодействии с активными металлами (чаще цинковая пыль или порошок магния) при нагревании:
Получи больше пользы от Skysmart:
-
Подготовься к ОГЭ на пятёрку
-
Подготовься к ЕГЭ на высокие баллы
Записывайся на бесплатные курсы для детей
Решай задания в бесплатном тренажёре ЕГЭ
Применение алкенов
Применение алкенов - это использование этих непредельных углеводородов в различных химических и промышленных процессах. Алкены необходимы для:
- Производства пластмасс (полиэтилен, полипропилен)
- Изготовления синтетических волокон
- Получения спиртов (этиловый спирт)
- Синтеза карбоновых кислот, альдегидов и кетонов
Пример: этилен ускоряет созревание плодов в теплицах.
Алкены не используют в качестве топлива из-за их высокой химической активности. Низшие алкены часто применяют в качестве исходного сырья для получения различных веществ. Наиболее широко используется этен. Вот что из него производят:
этиленгликоль — компонент антифриза и взрывчатых веществ;
этиленоксид — входит в состав моющих средств, синтетических волокон и других товаров народного потребления;
хлорэтан — входит в состав анестезирующих веществ;
дихлорэтан — используется как растворитель;
этанол — применяется в производстве чистящих и моющих средств, антифриза и омывающих жидкостей, а также синтетического каучука;
полиэтилен — используется для производства пластмасс;
уксусный альдегид, уксусную кислоту, дивинилхлорид и другие вещества.
Этилен активно используется, чтобы ускорить созревание неспелых бананов: перед тем как поступить в продажу, зеленые бананы в течение длительного времени находятся в атмосфере этилена.
Изучать химические свойства, получение и применение алкенов гораздо интереснее на примерах из окружающего мира — так считают методисты и преподаватели онлайн-школы Skysmart. Если вы с нами согласны, приводите ребенка на онлайн-курсы по химии, и мы поможем ему или ей искренне полюбить этот предмет, повысить средний балл в школе и подготовиться к экзаменам.